Entendemos que la humanización de anticuerpos es una de las etapas más críticas en su camino a la industria. Esta es la razón por la que nuestros expertos son algunos de los científicos de mayor renombre en este campo y cuentan con una trayectoria admirable. 3 anticuerpos terapéuticos en el mercado y más de 30 en las fases clínica y preclínica son algunas de nuestras cifras clave. Consideramos que cada nueva inmunización de un anticuerpo monoclonal es un reto único y apasionante para llevar su compuesto a la fase clínica
¿Por qué elegir ProteoGenix para la humanización
de su anticuerpo monoclonal?

Expertos reconocidos en la humanización de anticuerpos
Cuente con expertos con más de 25 años de experiencia y una trayectoria inigualable en la humanización de anticuerpos.

Modelado tridimensional
Nuestra plataforma de modelado molecular tridimensional garantiza la conservación de la función biológica..

Sin derechos de la propiedad intelectual
Los anticuerpos humanizados serán íntegramente se su propiedad.

Servicios de caracterización integrales
ELISA, determinación de la KD frente a antígenos solubles o antígenos expresados en la superficie celular, estabilidad térmica, tasa de agregación, CI50,…

XtenCHOTM
¡Benefíciese del sistema de expresión transitoria más productivo del mercado para producir todas sus variantes de anticuerpos monoclonales humanizados!

Diversidad de formatos
Optimizamos la secuencia o humanizamos todos los formatos de anticuerpos: IgG de longitud completa, scFv, Fab, VHH (nanocuerpos),…
Nuestro proceso de humanización de anticuerpos monoclonales

- Secuenciación de anticuerpos partiendo de una línea celular de hibridoma
– Extracción y purificación de ARN
– Transcripción inversa
– Amplificación por PCR
– Secuenciación

- Evaluación de la bioactividad de anticuerpos quiméricos
– Síntesis de genes, incluyendo optimización de codones
– Subclonación en un vector de expresión
– Producción y purificación de anticuerpos quiméricos
– Análisis de control de calidad:
Go/No Go1

- Diseño de anticuerpos monoclonales humanizados
– Identificación de retromutaciones mediante modelado molecular tridimensional
– Selección de las líneas germinales humanas más relevantes
– Injerto de CDR y optimización de secuencias asistidos por ordenador
Go/No Go2

- Producción de anticuerpo humanizado (de 9 a 18 variantes)
– Síntesis de genes, incluyendo optimización de codones
– Subclonación en un vector de expresión
– Transfección, expresión y purificación transitorias
– Análisis de control de calidad:
Go/No Go3

- Caracterización de las variantes humanizadas
– ELISA frente a antígeno
– Afinidad del anticuerpo frente a antígeno soluble o antígeno expresado en la superficie celular
– Tasa de agregación
– Estabilidad térmica
– Perfil de glicosilación
– Detección de endotoxina
Nuestro servicio de humanización de anticuerpos monoclonales
| Etapa | Contenido | Plazo | Resultados |
|---|---|---|---|
| Secuenciación del anticuerpo parental a partir de hibridomas |
|
~2-3 semanas |
|
| Expresión y purificación de anticuerpo quimérico |
|
~7-9 semanas |
|
| Diseño del anticuerpo humanizado |
|
~2 semanas |
|
| Producción recombinante transitoria de 9 a 18 variantes de anticuerpo |
|
~7-9 semanas |
|
| Caracterización de las variantes de anticuerpo monoclonal humanizado |
|
A determinar |
|
|
Opciones disponibles:
|
|||
¿Qué factores se deben tener en cuenta en la humanización de anticuerpos monoclonales?
El principal objetivo del proceso de humanización de anticuerpos es desarrollar una secuencia de anticuerpo que cumpla con las directrices de la Organización Mundial de la Salud (OMS) para anticuerpos humanizados. Básicamente, un anticuerpo se considera humanizado cuando la identidad de secuencia entre el anticuerpo y una secuencia de la línea germinal humana (de la base de datos IMGT) es de al menos un 85 %. La diferencia entre un anticuerpo humanizado y un anticuerpo totalmente humano radica en el origen del anticuerpo; los anticuerpos que proceden de especies no humanas se clasificarán como humanizados después de su humanización, mientras que las secuencias procedentes de humanos se considerarán «anticuerpos totalmente humanos».
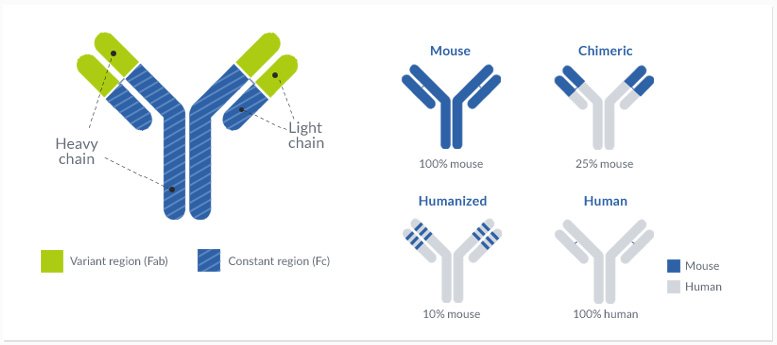
Para alcanzar este objetivo del 85 %, es necesario modificar la secuencia del anticuerpo en las regiones variables. Por consiguiente, este trabajo de ingeniería de anticuerpos puede tener un impacto crítico sobre las propiedades fisicoquímicas y farmacológicas del producto final y debe realizarse meticulosamente. Por este motivo, ProteoGenix aúna sus inigualables conocimientos técnicos en ingeniería de anticuerpos y su equipo de expertos, con más de 25 años de experiencia y una impresionante trayectoria en la humanización de anticuerpos. Nuestro proceso de humanización abarca el injerto de CDR, el modelado molecular y la optimización de la secuenciación.
El modelado molecular es una parte importante de este proceso, ya que permite analizar las contribuciones de los aminoácidos localizados en los bucles hipervariables (CDR) y en las regiones marco. Esta etapa es esencial para identificar qué residuos se pueden seleccionar para realizar las retromutaciones y cuáles se pueden mutar para la optimización adicional de diversas propiedades. Los aminoácidos implicados en las regiones variables se pueden clasificar como se indica a continuación:
-
residuos implicados en la interacción anticuerpo-antígeno,
-
residuos que desempeñan una función estructural, por ejemplo, mantener la conformación del bucle hipervariable (CDR) o estabilizarla interacciónVL VH-V,L,
-
residuos que interactúan con el disolvente.
Los residuos de las regiones marco murinas que se consideren críticos para mantener la conformación de los bucles hipervariables (CDR) y la bioactividad del anticuerpo, se retromutarán en las líneas germinales humanas seleccionadas.
La selección de la línea germinal humana se basa en la homología de secuencia, pero se pueden ensayar otras variantes de humanización que presenten una homología de secuencia inferior y buenas propiedades fisicoquímicas. En un proyecto de humanización, ProteoGenix selecciona varias cadenas pesadas y ligeras con el fin de generar entre 9 y 18 combinaciones..
Los diferentes anticuerpos generados se caracterizan y comparan posteriormente con el anticuerpo parental y/o quimérico de referencia con el fin de evaluar:
-
la inmunogenicidad,
-
sus propiedades fisicoquímicas (estabilidad, tasa de agregación,…),
-
sus propiedades farmacológicas (afinidad, especificidad,…)
-
su potencial de fabricación.
Tras superar los ensayos con éxito, se pueden seleccionar los prototipos candidatos para su posterior humanización y/u optimización de secuencias CDR con el fin de mejorar sus propiedades biofísicas (heterogenicidad, fragmentación, agregación,…) y su potencial de fabricación (bioproducción).
Se pueden ofrecer servicios de maduración de la afinidad integrales mediante presentación en fagos utilizando librerías personalizadas generadas mediante mutagénesis aleatoria o dirigida.





