Wir sind uns bewusst, dass die Antikörperhumanisierung zu den kritischsten Schritten auf Ihrem Weg zur klinischen Prüferlaubnis zählt. Deshalb gehören unsere Experten zu den renommiertesten Wissenschaftlern auf diesem Gebiet und können eine beeindruckende Erfolgsbilanz vorweisen, unter anderem 3 zugelassene therapeutische Antikörper sowie über 30 Antikörper, die in der präklinischen oder klinischen Prüfung befinden. Für uns ist jede Humanisierung eines neuen monoklonalen Antikörpers ein Teil der einzigartigen und spannenden Herausforderung, Ihr Molekül in die klinische Phase zu bringen.
Warum ist ProteoGenix der richtige Partner für die
Humanisierung Ihres monoklonalen Antikörpers?

Anerkannte Experten für die Antikörperhumanisierung
Sichern Sie sich Zugang zu Experten mit mehr als 25 Jahren Erfahrung in der Antikörperhumanisierung..

3D-Modellierung
Unsere 3D-Molekülmodellierungsplattform garantiert den Erhalt der biologischen Funktion.

IP-frei
Die humanisierten Antikörper gehen vollständig in Ihr Eigentum über.

Umfassende Charakterisierungsservices
ELISA, KD-Bestimmung gegen lösliches Antigen oder Zellen, Thermostabilität, Aggregationsrate, IC50 …

XtenCHOTM
Profitieren Sie vom produktivsten transienten Expressionssystem, mit dem sich alle Varianten Ihres humanisierten monoklonalen Antikörpers erzeugen lassen.

Formatvielfalt
Wir führen Sequenzoptimierung oder Humanisierung aller Arten von Antikörperformaten durch: vollständiges IgG, scFv, Fab, VHH (Nanobodies) …
Unser Prozess zur Humanisierung von monoklonalen Antikörpern

- Antikörpersequenzierung ausgehend von der Hybridomazelllinie
– RNA-Extraktion und -Aufreinigung
– Reversen Transkription
– PCR-Amplifikation
– Sequenzierung

- Bewertung der Bioaktivität von chimärischen Antikörpern
– Gensynthese mit Codon-Optimierung
– Subklonierung in Expressionsvektor
– Herstellung und Aufreinigung von chimärischen Antikörpern
– QK-Analyse
Go/No Go1

- Design von humanisierten monoklonalen Antikörpern
– Identifikation von Rückmutationen mittels 3D-Molekülmodellierung
– Selektion der humanen Keimbahnen mit der höchsten Relevanz
– In-silico-CDR-Grafting und Sequenzoptimierung
Go/No Go2

- Herstellung der humanisierten Antikörper (9–18 Varianten)
– Gensynthese mit Codon-Optimierung
– Subklonierung in Expressionsvektor
– Transiente Transfektion, Expression und Aufreinigung
– QK-Analyse
Go/No Go3

- Charakterisierung der humanisierten Varianten
– ELISA gegen Antigen
– Antikörperaffinität gegen lösliches Antigen oder Zelle
– Aggregationsrate
– Thermostabilität
– Glykosylierungsprofil
– Endotoxinbestimmung
Leistungsumfang unserer Services für die Humanisierung von monoklonalen Antikörpern
| Schritt | Leistungen | Zeitrahmen | Lieferumfang |
|---|---|---|---|
| Elternantikörper-Sequenzierung aus Hybridoma |
|
ca. 2–3 Wochen |
|
| Herstellung und Aufreinigung von chimärischen Antikörpern |
|
ca. 7–9 Wochen |
|
| Design des humanisierten Antikörpers |
|
ca. 2 Wochen |
|
| Transiente rekombinante Produktion von 9 bis 18 humanisierten Antikörpervarianten |
|
ca. 7–9 Wochen |
|
| Charakterisierung der humanisierten monoklonalen Antikörpervarianten |
|
Noch festzulegen |
|
|
Verfügbare Optionen:
|
|||
Welche Faktoren sind bei der Humanisierung monoklonaler Antikörper zu beachten?
Die Humanisierung von Antikörpern dient in erster Linie dazu, eine Antikörpersequenz zu erhalten, die den Leitlinien der Weltgesundheitsorganisation (WHO) für humanisierte Antikörper entspricht. Grundsätzlich gilt ein Antikörper als humanisiert, wenn die Sequenzübereinstimmung zwischen dem Antikörper und einer humanen Keimbahn (aus der IMGT-Datenbank) mindestens 85 % beträgt. Der Unterschied zwischen humanisiert und vollhuman hängt von der Herkunft des Antikörpers ab: Antikörper aus nichthumanen Spezies werden nach der Humanisierung als „humanisiert“ eingestuft, während Sequenzen menschlichen Ursprungs als „vollhuman“ gelten.
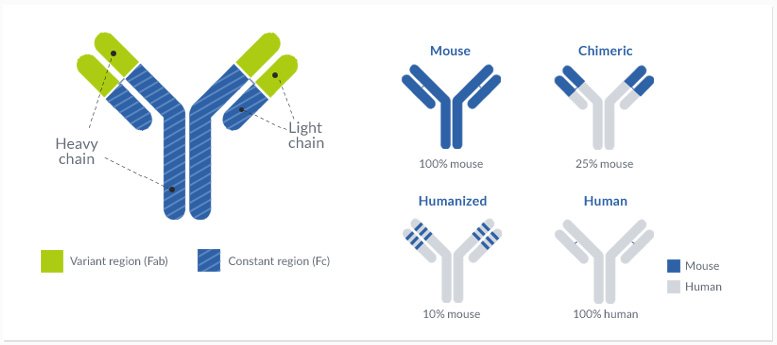
Zum Erreichen des 85-%-Ziels ist eine Modifikation der Antikörpersequenz in den variablen Regionen nötig. Somit kann das Antikörper-Engineering einen entscheidenden Einfluss auf die physikalisch-chemischen und pharmakologischen Eigenschaften des Endprodukts haben und sollte sorgfältig durchgeführt werden. ProteoGenix kombiniert deshalb sein unübertroffenes Know-how im Bereich Antikörper-Engineering mit Experten, die über mehr als 25 Jahre Erfahrung verfügen und eine beachtliche Erfolgsbilanz in der Antikörperhumanisierung vorweisen können. Unser Humanisierungsprozess umfasst CDR-Grafting, Molekülmodellierung und Sequenzoptimierung.
Die Molekülmodellierung ist ein wichtiger Prozessbestandteil, da sie es ermöglicht, den Anteil der einzelnen Aminosäuren in den murinen CDR-Schleifen und in Framework-Regionen zu analysieren. Dieser Schritt ist unerlässlich, um für Rückmutationen geeignete Reste sowie solche, die zur weiteren Optimierung der Eigenschaften mutiert werden können, zu bestimmen. Die Aminosäuren der variablen Regionen können wie folgt eingeteilt werden:
-
Reste, die an der Antikörper-Antigen-Wechselwirkung beteiligt sind
-
Reste mit struktureller Funktion, beispielsweise Aufrechterhaltung der CDR-Schleifenkonformation oder Stabilisierung der VH-VL -Wechselwirkung
-
Reste, die mit dem Lösungsmittel interagieren
Reste aus den murinen Framework-Regionen, die als kritisch für die Aufrechterhaltung der CDR-Schleifenkonformation und der Antikörper-Bioaktivität eingestuft werden, werden in die selektierten humanen Keimbahnen rückmutiert.
Die Selektion der humanen Keimbahnen basiert auf der Sequenzhomologie, es können jedoch auch andere Humanisierungsvarianten getestet werden, die eine geringere Sequenzhomologie, aber gute physikalisch-chemische Eigenschaften aufweisen. In einem Humanisierungsprojekt selektiert ProteoGenix verschiedene schwere und leichte Ketten, um 9 bis 18 Kombinationen zu generieren.
Die verschiedenen generierten Antikörper werden genauer charakterisiert und mit dem Eltern- und/oder chimärischen Referenzantikörper verglichen, um folgende Eigenschaften zu beurteilen:
-
Immunogenität
-
physikalisch-chemische Eigenschaften (Stabilität, Aggregationsrate, …)
-
pharmakologische Eigenschaften (Affinität, Spezifität, …)
-
Herstellbarkeit
Nach erfolgreichen Tests können Antikörperkandidaten für die weitere Humanisierung und/oder CDR-Sequenzoptimierung zwecks Verbesserung der biophysikalischen Eigenschaften (Heterogenität, Fragmentierung, Aggregation, …) und der Herstellbarkeit (Bioproduktion) selektiert werden.
Umfassende Services für die Antikörper-Affinitätsreifung können mittels Phagen-Display unter Verwendung kundenspezifischer, per zufälliger oder Target-Mutagenese erzeugter Bibliotheken realisiert werden.





