Cart (0 Items)
Your cart is currently empty.
View ProductsYou're visiting from outside the EU. Switch to the US version to see local pricing and tax details in USD.
Switch to US ($)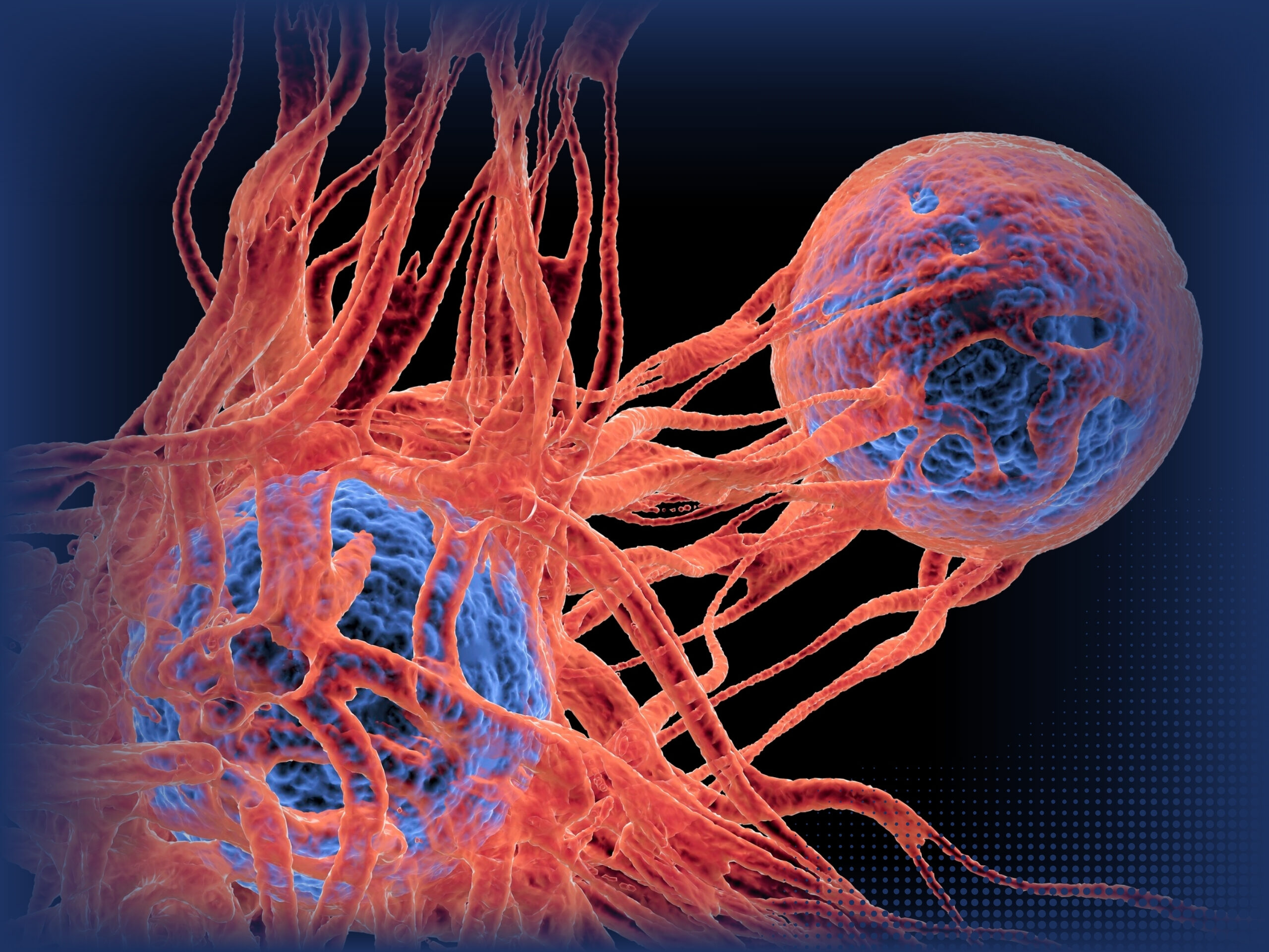
Creada a partir de dos fuentes, nuestra biblioteca captura hasta el 90% de las células B humanas productoras de anticuerpos. Esto garantiza acceso a dianas clínicamente relevantes, incluyendo autoantígenos, neoantígenos y complejos MHC–péptido y numerosos objetivos a los que las bibliotecas sintéticas no pueden llegar.
LiAb-SFCANCER™ se compone de 86 pacientes oncológicos de 18 indicaciones, proporcionando un repertorio excepcionalmente diverso: 6,81×10¹⁰ clones scFv y 6,72×10¹⁰ clones Fab.
Nuestra biblioteca de phage display incluye neoplasias raras—leucemia linfoblástica B (B-ALL), linfoma linfoblástico B (B-LL) y mieloma múltiple— caracterizadas por una alta proliferación de células pre-B que reconocen autoantígenos, haciendo de LiAb-SFCANCER™ una biblioteca única en el mundo.
Entregamos al menos tres uniones validadas, proporcionándole candidatos de respaldo para asegurar su éxito.
Ahorre tiempo valioso con un flujo de trabajo optimizado del diseño de secuencia a anticuerpo, sin sacrificar calidad ni rendimiento.
Sin regalías ni tarifas de licencia, usted mantiene el control total sobre el desarrollo posterior.
Vea cómo esta exclusiva biblioteca acelera el progreso en diferentes usos oncológicos. Al proporcionar anticuerpos humanos específicos de cáncer con bajos requerimientos de ingeniería y mínimo riesgo de inmunogenicidad, usted acelera el desarrollo de su anticuerpo contra dianas difíciles y su transición a la etapa preclínica.
Descubra cómo diseñamos un anticuerpo contra una diana apenas visible para el sistema inmune.
Descubra cómo la tecnología innovadora de phage display, impulsada por nuestra biblioteca de pacientes oncológicos, acelera el desarrollo de nuevos fármacos al tiempo que ahorra tiempo y reduce el uso de animales.
Conozca la importancia de nuestra biblioteca LiAb-SFCANCERTM para el desarrollo de anticuerpos contra antígenos tumorales.
